Das Forschungslabor der Klinik und Poliklinik für Mund-, Kiefer- und Gesichtschirurgie beschäftigt sich schwerpunktmäßig mit Knochen Tissue Engineering. Wir arbeiten mit Kieferperiostzellen als „vorgeprägte“ Stammzellquelle und charakterisieren diese in Detail [2-20]. Für diesen Zelltyp geeignete, Biomaterialien werden identifiziert, mit Molekülen funktionalisiert, die eine natürliche Mikroumgebung nachahmen sollen und auf ihre Biokompatibilität untersucht.
Forschung
Knochen Tissue Engineering
In Deutschland wird jährlich bei mehr als 10.000 Patienten ein Mundhöhlenkarzinom diagnostiziert [1]. Die daraus resultierende Kieferknochenresektion verursacht z.T. große Knochendefekte, die wieder rekonstruiert werden müssen. Für das Standardverfahren der autologen Knochentransplantation wird eine schonendere Alternative gesucht. Der zukunftsorientierte Bereich des Tissue Engineerings stellt eine vielversprechende therapeutische Alternative, die sich die körpereigene Regenerationskraft zunutze macht, um verloren gegangene Gewebefunktionen zu ersetzen. Dieses Verfahren beinhaltet patienteneigene Stammzellen, die optimal für den Zelltyp, der gebraucht wird, prädestiniert sind. Für die Generierung von dreidimensionalen Konstrukten, wachsen die Stammzellen in geeigneten 3D Gerüstmaterialien.
Kontakt
frontend.sr-only_#{element.icon}: Prof. Dr. Dorothea Alexander-Friedrich Laborleitung
frontend.sr-only_#{element.icon}: 07071 29-82418
frontend.sr-only_#{element.icon}: 07071 29-4365
E-Mail-Adresse: Dorothea.Alexander@med.uni-tuebingen.de
Mehr zur Person
Forschungsprojekte
- Generierung von induzierten, pluripotenten Stammzellen aus Kieferperiostzellen
- Immunogenität von JPCs / JPC-besiedelten Konstrukten
- Qualitätsanalyse der während der in vitro JPC-Osteogenese gebildeten Extrazellulärmatrix
- Identifizierung von spezifischen Oberflächenmarkern für die osteogenen Vorläuferzellen aus dem Kieferperiost
- Identifizierung und Funktionalisierung eines optimalen Gerüstmaterials für JPCs
- Effects of dexamethasone on JPC expression and osteogenic differentiation patterns
- Histological embedding methods and histological/immunohistological stainings of JPC-seeded scaffolds
- Interactions between JPCs and osteoclasts
- Practical work experience
Kooperation Herz-Thorax-Chirurgie - Generierung von induzierten, pluripotenten Stammzellen aus Kieferperiostzellen
DFG-Projekt / Kooperation Herz-Thorax-Chirurgie - Generierung von induzierten, pluripotenten Stammzellen aus Kieferperiostzellen
Die Wiederherstellung von großen Knochendefekten mit KTE Konstrukten bei z.B. Tumorpatienten, braucht extrem hohe Stammzellzahlen. Leider ist die Generierung von hohen Zellzahlen durch das Vorkommen der Zellseneszenz sowie den Rückgang des osteogenen Potentials in hohen Zellpassagen, stark erschwert. Zusätzlich zeigen primäre Kieferperiostzellen unter Kultivierung mit fötalem Kälberserum sehr große Unterschiede bzgl. des osteogenen Potentials.
Obwohl Oberflächenmarker für die Sortierung von Vorläuferzellen aus dem Kieferperiost per FACS oder MACS identifiziert wurden, sind die resultierenden Zellausbeuten stets unbefriedigend und von einer hohen Zellmortalität begleitet.
Die Verwendung von Patienten-spezifischen induzierten pluripotenten Stammzellen (iPSCs), von somatischen Zellen ausgehend, kann die genannten Probleme lösen. In der vorliegenden Studie verwendeten wir für die Reprogrammierung von Kieferperiostzellen ein selbst-replizierendes RNA-Konstrukt, das eine GFP-kodierende Sequenz für ein direktes Live-Monitoring, enthält. Die anschließende Differenzierung von iPSCs zu iMSCs kann zur Generierung einer homogeneren Zellpopulation führen, die zur Standardisierung des TE-Prozesses beitragen könnte.
(PhD student Felix Umrath, Doctoral student Sarah-Lena Frick)
Immunogenicity of JPCs / JPC-seeded constructs
Immunogenität von JPCs / JPC-besiedelten Konstrukten
Die Biokompatibilität der in vitro generierten Tissue Engineering Konstrukte müssen vor der Anwendung im Patienten getestet werden. Je nach Materialeigenschaften bzw. nach Interaktionen zwischen Stammzellen und Biomaterial, können diese in vivo eine Immunreaktion auslösen.
Um eine zuverlässige Aussage über die Verträglichkeit der entwickelten Knochen-Konstrukte machen zu können, untersuchen wir die Interaktion zwischen JPCs oder JPC-besiedelte Konstrukten und Zellen des Immunsystems (dendritische Zellen, Makrophagen) in der Ko-Kultur.
Following projects are partially sponsored by China Scholarship Council:
- Effects of jaw periosteal cells on the maturation of dendritic cells (PhD student Jingtao Dai)
- Influence of jaw periosteal cells on macrophage differentiation in the two- and three-dimensional (Doctoral student Fang He)
- Establishment of a dynamic co-culture system for the testing of biocompatibility of BTE constructs (Doctoral student Wanjing Cen)
Qualitätsanalyse der während der in vitro JPC-Osteogenese gebildeten Extrazellulärmatrix
Qualitätsanalyse der während der in vitro JPC-Osteogenese gebildeten Extrazellulärmatrix
Die klinische Applikation von in vitro hergestellten TE-Konstrukten beim Menschen, setzt eine Standardisierung des Fabrikationsprozesses voraus. In puncto Biomaterialien erlaubt die innovative 3D-Drucktechnologie, ein hohes Level an Präzision und Gleichmäßigkeit der Druckqualität, die zu einem standardisierten Herstellungsprozess führt.
Material-Modifikationen mit funktionellen Bio-Molekülen um Zellfunktionen zu verstärken bzw. zu kontrollieren, erfordert geeignete Detektionsmethoden, die nicht ausreichend etabliert sind. Gleichzeitig muss für die Qualitätskontrolle die Reifung der generierten Zell-Material Konstrukte schrittweise überwacht und kontrolliert werden, um den optimalen Zeitpunkt zu bestimmen, an dem die BTE-Produkte eingesetzt werden können bzw. um den Erfolg des angewendeten TE-Verfahres zu sichern.
Kieferperiostzellen sind in der Lage nach Stimulation mit bestimmten Reagenzien eine Knochen-spezifische Matrix zu bilden. Die Zellmineralisation kann mittels histologischer Färbungen nachgewiesen und quantifiziert werden. Es können jedoch keine Aussagen über die Qualität der gebildeten Matrix gemacht werden. Mithilfe der Raman Technologie kann eine nicht-destruktive Analyse erfolgen. Basierend auf entsprechenden Molekülvibrationen, werden Fingerprint Raman Spektren generiert, die eine biochemische Analyse der gebildeten Matrix, erlaubt. Die biochemische Charakterisierung der mineralisierten Matrix enthält Informationen über Struktur und Funktion des gebildeten Gewebes und hilft bei der Klassifizierung bzw. Diskriminierung von qualitativ schlechtem Knochengewebe.
Vergleich der von Kieferperiostzellen gebildeten Knochen-spezifischen Matrix unter Serum-haltigen und –freien Kulturbedingungen
DFG-Förderung Die Unterschiede in der biochemischen Zusammensetzung der von der MSCA-1+ JPC-Subpopulation gebildeten Kristalle unter Serum-haltigen und Serum-freien Kulturbedingungen wurden in dieser Studie analysiert. MSCA-1+ JPCs bilden unter Serum-freien Bedingungen eine reifere Knochen-ähnliche Matrix mit vermutlich schlechteren elastischen Eigenschaften, basierend auf der reduzierten Kollagenproduktion der Zellen.

Vergleich der von Kieferperiostzellen gebildeten EZM unter FCS und –hPL Supplementierung
In dieser Studie haben wir die Rasterkraftmikroskopie kombiniert mit der Raman Technologie angewendet, um gleichzeitig Aussagen über die mechanischen und biochemischen Eigenschaften der gebildeten mineralisierten Matrix, machen zu können. Da es für eine spätere klinische Applikation wichtig ist, auf tierische Komponenten bei der in vitro Zellkultur zu verzichten, untersuchten wir in dieser Studie die gebildete Zellmatrix unter FCS- und Plättchenlysat-Supplementierung. Wir konnten eine qualitativ-hochwertigere Matrix unter Plättchenlysat-Supplementierung nachweisen [15].

Identifizierung von spezifischen Oberflächenmarkern für die osteogenen Vorläuferzellen aus dem Kieferperiost
Identifizierung von spezifischen Oberflächenmarkern für die osteogenen Vorläuferzellen aus dem Kieferperiost
BMBF Förderung Das Kieferperiost ist ein sehr dünnes, zwei-schichtiges Gewebe. Die äußere Schicht enthält hauptsächlich Gewebsfibroblasten und kollagenöse Fasern, während die innere, dem Knochen zugewandte Zellschicht hauptsächlich die osteogenen Vorläuferzellen enthält. Unsere in vitro Zellkultur besteht aus einer Mischpopulation, die Zellen aus beiden Schichten enthält, da eine mechanische Trennung beider Schichten nicht möglich ist.
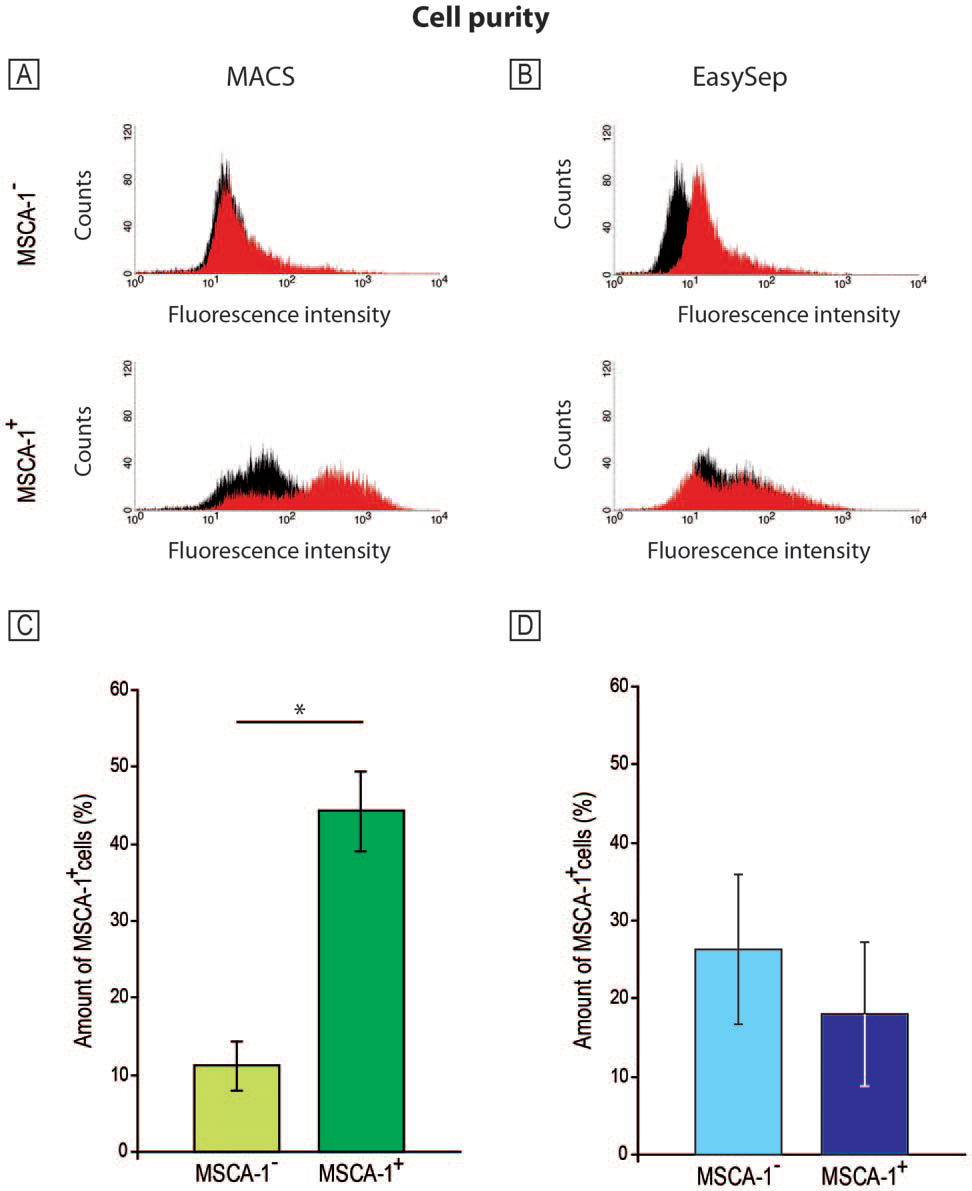
Wir identifizierten „mesenchymal stem cell antigen-1“ (MSCA-1) als spezifischen Marker für die Subpopulation mit dem stärksten osteogenen Potential [8]. Somit kann die MSCA-1 positive Subpopulation aus der gesamten Zellpopulation isoliert werden [16, 19]. Leider wird sowohl die Fluoreszenz- als auch die magnetisch-aktivierte Zellsortierung mithilfe dieses Markers von einer hohen Mortalität begleitet. Interessanterweise erfolgte durch die in vitro Kultivierung mit einem Serum-freien Medium eine gewisse Selektion der MSCA-1+ Subpopulation [6].
Identifizierung und Funktionalisierung eines optimalen Gerüstmaterials für JPCs
Identifizierung und Funktionalisierung eines optimalen Gerüstmaterials für JPCs
Verschiedene degradierbare Biomaterialien werden auf ihre Eignung für Kieferperiostzellen analysiert [5].
AiF Förderung / DFG sponsoring Um den Zellen eine natürliche Mikroumgebung auf den synthetisch-hergestellten Biomaterialien zu simulieren, werden diese durch verschiedene Strategien biofunktionalisiert [9-12].

Effects of dexamethasone on JPC expression and osteogenic differentiation patterns
Effects of dexamethasone on JPC expression and osteogenic differentiation patterns
(Doctoral student Achim Pfeifer)
Histological embedding methods and histological/immunohistological stainings of JPC-seeded scaffolds
Bachelor thesis for Medical Technology (Bachelor student Lukas-Frank Schmitt)
Interactions between JPCs and osteoclasts
Master thesis for Medical Technology (Master student Alena Fischer)
Practical work experience
Cooperation with the University of Sassari/Sardinia (Erasmus student Stefano Carta)
Zertifikate und Verbände

Focus: Top Nationales Krankenhaus 2025

Stern: Deutschlands Ausgezeichnete Arbeitgeber Pflege 24/25

Qualitätspartnerschaft mit der PKV

Erfolgsfaktor Familie

Die Altersvorsorge für den Öffentlichen Dienst






